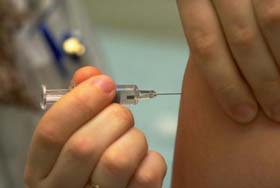
Après quelque 100.000 vaccinations de personnels de santé contre la grippe H1N1, 91 cas d’effets indésirables ont été signalés dont quatre cas « graves » qui ont nécessité une hospitalisation, indique vendredi l’Agence de sécurité sanitaire des produits de santé (Afssaps).
Dans son bulletin de suivi de pharmacovigilance des vaccins couvrant la période 21 octobre/10 novembre, où seuls les professionnels de santé pouvaient être vaccinés, l’Afssaps note que la majorité des cas rapportés a été « d’intensité bénigne à modérée ».
Tous ont reçu une injection du vaccin Pandemrix de GlaxoSmithKline, le seul actuellement disponible en France.
Les quatre cas d’effets « graves » concernent deux affections neurologiques (dont le cas « probable » de syndrome de Guillain-Barré cité jeudi par le ministère de la Santé), une réaction allergique et une affection respiratoire.
Un homme de 34 ans, qui avait déjà souffert il y a 12 ans de « troubles neurologiques à type de paresthésie » avec engourdissement des membres inférieurs, a présenté des signes cliniques comparables trois jours après l’injection du vaccin. Des examens sont en cours pour établir la cause, le patient est toujours hospitalisé et son état « s’améliore ».
La femme de 37 ans soupçonnée d’être atteinte du syndrome de Guillain-Barré n’avait pas d’« antécédents médicaux particuliers ». Elle a présenté « des paresthésies (fourmillements, troubles de sensibilité), ascendantes des pieds jusqu’au cou et irradiant vers les membres supérieurs, six jours après la vaccination ».
« Une régression des signes cliniques après échanges plasmatiques en hôpital de jour a permis son retour à domicile », indique l’Afssaps. « Un diagnostic de syndrome de Guillain-Barré de forme modérée est suspecté » mais des examens sont en cours pour établir la cause.
L’Afssaps rappelle que le risque de Guillain-Barré « augmente lorsqu’on est atteint de la grippe ».
Un oedème de Quincke chez une femme de 26 ans
Le troisième cas est « une réaction allergique à type d’oedème de Quincke » survenue juste après la vaccination chez une femme de 26 ans « sans aucun antécédent personnel ou familial d’allergie », dont l’état « s’améliore sans aucune séquelle sous traitement adapté ». « De tels effets indésirables sont attendus pour beaucoup des vaccins », indique l’Afssaps.
Enfin une femme de 30 ans, « avec des antécédents médicaux d’allergie aux poils de chat », a présenté un tableau clinique associant spasme des bronches, essoufflement, fièvre et urticaire le soir de la vaccination. « Son état s’améliore sous traitement adapté », précise l’Afssaps.
82 cas « « non graves »
Les cinq autres cas « jugés médicalement significatifs » (trois cas de malaise associé à une augmentation de la pression sanguine, un cas de sensation vertigineuse et un cas de douleur intense au site d’injection) n’ont nécessité qu’une « simple surveillance ».
Les 82 signalements d’effets indésirables « non graves » sont des réactions au site d’injection (douleur, induration, oedème), des réactions allergiques (érythèmes, urticaire), des réactions plus générales (fièvre, maux de tête, fatigue ou syndrome grippal).
« La plupart des cas déclarés au système de pharmacovigilance correspondent à des effets attendus de ce vaccin », indique l’Afssaps, et « ne remettent pas en cause la balance bénéfice-risque du Pandemrix ».
Les effets indésirables peuvent être déclarés par des professionnels de santé ou par des patients sur des formulaires de déclaration disponibles sur le site de l’Agence . Ils sont évalués médicalement avant d’être validés.











 et
et  !
!